非小细胞肺癌靶向药物盘点2016-11-11首要死亡原因 肺癌是首要的死亡原因之一,全球每年有140万人死于肺癌,NSCLC则占到肺癌总人群的85%。自从EGFR靶向药物应用以来,NSCLC的治疗迎来了颠覆性的变化。
在含铂化疗时代,晚期NSCLC的中位生存期只有8个月,以EGFR抑制剂为代表的靶向药物则彻底改变了这一格局(亚洲人的EGFR突变率更高,达到30-50%)。然而,靶向药物也因耐药等问题催生了快速迭代,临床仍有极大的未满足需求。PD-1/PD-L1抑制剂的出现,使得NSCLC的治疗再次面临新的变化,免疫疗法或将成为NSCLC最重要的治疗手段。中国是肺癌多发国家,据统计全国有超过500万肺癌患者,每年新发病例超过73万人,死亡人数超过60万人。
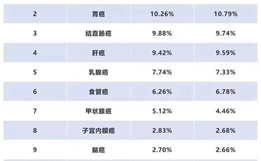
中国是肺癌多发国家,据统计全国有超过500万肺癌患者,每年新发病例超过73万人,死亡人数超过60万人。
▲数据来自:中国肿瘤登记中心2015年报基因突变分型 下图为肺癌基因突变分型,数据来自KUMARAKULASINGHE 2015年的文章“Molecular targeted therapy in the treatment of advanced stage non-small cell lung cancer (NSCLC)”。
▲数据来源:Respirology (2015) 20, 370–378 doi:10.1111/resp.12490 肺腺癌占到NSCLC患者总人群的50%以上,是最常见的组织亚型,主要基因突变类型包括: KRAS、EGFR、BRAF、HER2、PIK3CA、MET 基因突变和 ALK、ROS1 和 RET 基因重排。
肺鳞癌占到NSCLC患者总人群的20%左右,主要基因突变类型包括:成纤维细胞生长因子受体 -1(FGFR1)的基因扩增,盘状结构域受体 2(DDR2)基因突变和 PI3KCA 基因的扩增和突变等。 亚洲人EGFR突变比例远高于上述比例,达到50%左右。
根据经阐明的分子遗传学机制,药企开发了多个靶向药物。
在研药物中,第三代EGFR靶向药物和免疫疗法PD-1/PD-L1抗体的竞争最为激烈。Tagrisso成为首个上市的三代EGFR靶向药物,Keytruda成为首个一线免疫疗法。
此外还有多种新机制的药物被开发用于NSCLC的治疗,如癌症疫苗、PARP抑制剂、CDK4/6抑制剂等。随着靶向药物的广泛应用,耐药将同时催生更多的联合疗法,这里不再一一列举。靶向药物的研发历程 相较化疗药物,靶向药物的副作用更小,极大提高了病人的生存质量。
但靶向药物同样存在某些严重副作用,并且最终会耐药,病人不得不在靶向药物用尽的情况下,回到化疗药物。临床上,不断探索靶向药物耐药机制,进而推动药企研发相应的新靶向药物。这些努力给患者提供了更多选择,当然,也往往伴随诸多研发风险。这里以EGFR靶向药物为例,说明靶向药物的研发历程和发展方向。
EGFR靶向药物 厄洛替尼、吉非替尼等是EGFR突变阳性的一线治疗药物,但通常1-2年后,患者会出现耐药,这时候就需要换药。
耐药机制50%是因为发生了T790M突变,二代EGFR靶向药物如阿法替尼虽然活性更强,但对T790M特异性不强,对野生型EGFR的亲和力也很高,导致严重的副作用:皮疹和腹泻等。 在清楚了一代EGFR-TKI药物耐药机制后,药企前赴后继的开始了研发第三代针对EGFR T790M的新药,2015年,阿斯利康的Tagrisso(即AZD9291)获得FDA批准上市。
随着一线EGFR-TKI药物的广泛应用,这些患者最终都会产生耐药,应对T790M的突变就成为一个迫切的需求。
除了阿斯利康,Clovis Oncology、辉瑞、诺华、安斯泰来、韩美、CheckPoint、中国的艾森医药、华东医药等都在积极开发靶向EGFRT790M的药物。
表三 第三代EGFR靶向药物(T790M)表中艾森医药的艾维替尼与华东医药的迈华替尼同为十三五重大新药创制品种,希望同凯美纳一样,自主研发药物为患者带来更多选择,使得药物可及性切实提高。 Tagrisso等第三代EGFR靶向药物,在使用过程中会发生新的耐药,和三代药物本身的开发一样,仍需首先研究清楚耐药机制,进而开发新的靶向药物。
最近的研究已经初步发现一些三代EGFR靶向药物的耐药机制,如Tagrisso的主要耐药机制可能包括C797S的基因突变等,这些研究将成为下一代EGFR靶向药物开发的重要依据。▲三代EGFR抑制剂药物的耐药机制 耐药推动靶向药物迭代 靶向药物的治疗机制基于对癌细胞的特异性识别和杀伤,而癌细胞与细菌等微生物一样,会产生一系列耐药突变,使得药物失效。抗生素的滥用使得超级细菌泛滥,靶向药物的使用也需要谨慎对待,药物使用的次序、剂量和时间都需要严格控制,否则只会加速耐药。
在新药开发上,抗癌靶向药物比抗生素研发更为复杂,微生物与人体细胞成分极为不同,副作用相对容易控制。而癌细胞则来源于人体正常细胞,其成分和靶标与正常细胞差异很小,很难找到理想的靶标(癌细胞有而正常细胞完全没有),靶向也只能是相对性的。伴随而来的就是诸多严重的副作用。
这些因素都决定了靶向药物研发的复杂性。 表四抗菌药物与抗癌靶向药物的比较由于很多靶向药物新药尚未在国内上市,很多患者只能通过某些渠道购买原料药和辅料,自己灌装胶囊服用,如AZD9291、CO-1686、WZ4002,这些药企常用的研发代码成为癌症患者的熟悉名词。这些方法客观上起到了暂时控制病情的作用,但仍存在诸多风险。
一方面,原料药渠道、辅料、配制程序都存在一些不可控的风险,另一方面这些药物本身处于研究阶段,潜在安全性风险很大。如近日韩国韩美医药的第三代EGFR靶向药物HM61713就因为严重皮肤毒性导致2例死亡时间,不得不终止临床研究。面对类似的情况,患者仍需谨慎对待。
即便一些新的靶向药物最终在国内上市,高昂价格和保障力度薄弱的医保支付体系,使得许多患者望而兴叹。小编希望国内药企研发更多、更好、更便宜的新药,也希望医保支付体系能不断完善,惠及广大患者。免疫疗法快速发展 靶向药物还有很重要的一类:单克隆抗体药物尤其是免疫疗法如PD-1等。
如PD-1抗体药物在肺癌等适应症已经展现了强大的疗效。抗体药物都是注射剂,仿制和生产都极为复杂,只能等待药物在国内上市,或者参加临床研究。好在近年来国内抗体药物研发加速,恒瑞、百济神州、信达等多家药企开发的PD-1抗体药物陆续进入临床研究,给患者带来更多希望。
2016年9月,PD-1抗体药物Keytruda已经获得FDA批准成为治疗PD-L1高表达NSCLC患者的一线治疗药物。这将成为NSCLC治疗发展过程中的里程碑事件,免疫疗法或将成为NSCLC的最重要手段。根据Datamonitor Healthcare的估计,到2023年,PD-1/PD-L1抑制剂将成为最主要的NSCLC治疗药物。
参考资料: 1.Next-generation EGFR TKI in EGFR-mutant NCSLC(2016) 2.Third-generation inhibitors targeting EGFR T790M mutation in adavanced non-small cell lung cancer(2016) 3.The NSCLC market (2016) 4.Mechanisms of resistance to EGFR targeted drugs: lung cancer(2016) 5.Recent progress on third generation covalent EGFR inhibitors(2016) 6.中国肿瘤登记中心2015年报 7.Molecular targeted therapy in the treatment of advanced stage NSCLC(2015) 8.Second- and third-generation ALK inhibitors for non-small cell lung cancer(2016) 9.NCCN非小细胞肺癌治疗指南2015


曾任美国临床肿瘤学会(ASCO)临床实践指南委员会主席
约翰霍普金斯医学院,医学博士
Lifespan癌症研究所胸部肿瘤科主任
曾在纽约纪念斯隆凯特琳癌症中心任职10年
曾在波士顿的麻省总医院癌症中心任职6年

 400-107-6696
400-107-6696


 shower
shower
 12695
12695
 4
4

 13862
13862






 京公网安备 11010502037180号
京公网安备 11010502037180号
 400-107-6696
400-107-6696


