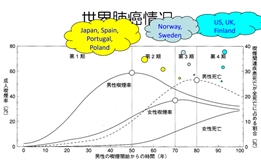
全世界范围内,肺癌的死亡率为诸类癌症之最。1966年,Peto等曾对44个发达国家的吸烟人群做了评估,他们认为由于吸烟导致的总死亡人数将在2020年以后超过1000万。最近数十年来,全球肺癌死亡率并无显著变化,其中2008年的肺癌死亡人数约为140万,其中中国的肺癌死亡人数增长速度特别值得关注。这与筛查及治疗方面已得到长足发展的癌症(颈部癌、乳腺癌、前列腺癌以及结直肠癌等)的情况有很大差异。肺癌发生率在已实施有效烟草控制的国家有明显下降,这表明肺癌发病率从政策介入开始到发病率下降需要约20年的时间来完成。然而,高龄前烟民中很大一部分均属于潜发肺癌的人群。当肺癌在有症状表现的情况下得到诊断时则预后很差,其总5年生存率在美国为16%;而在英国更低,男性甚至仅有7.8%,而女性则为9.1%。 技术原理 PET/CT 全身正电子发射断层扫描(PET)结合氟-18脱氧葡萄糖(FDG)是一项无创伤性检查。PET摄像机通过观测患者体内放射性示踪剂分布产生三维图像。目前PET扫描的空间分辨率大概为4mm,因此可以精确观察到大于8mm 的病灶。而葡萄糖类似物的FDG是目前临床肿瘤成像使用最多的代谢示踪剂。 PET扫描可以集合计算机断层成像(CT)技术或者磁共振(MR)技术。目前PET/CT扫描使用最为广泛,而PET/MR是一项新兴技术。联合使用PET 扫描与CT或MRI有三项最主要的优势:①CT 含有衰减矫正(AC)功能,可以矫正病人本身信号的干扰;②可以提高占位的精度,形态特征的关联性,减少单一PET不能明确的信号占位;③增强报告医生的信心。除非患者已有可用的增强CT,而PET/CT联合高剂量增强CT,能比单独的低剂量CT,更好地提供准确的TNM 分期诊断信息。 超声支气管镜引导下经支气管穿刺活检(EBUS-TBNA)和超声食管内镜引导下细针穿刺活检是常用的内镜穿刺技术。超声探头安置在内镜的顶部,内镜可以经此扫描中央气道或者食管深层结构,内镜连接超声系统,更好地分辨实质与血管结构。内镜附有专用针道,用于内镜超声下实时引导穿刺。超声内镜可以穿刺活检部分肺内占位、肺门或纵隔淋巴结。EBUS可穿刺第2R/2L、4R/4L、7组纵隔淋巴结,以及第10、11组甚至第12组淋巴结。EUS则用于上纵隔第4L组淋巴结,以及下纵隔的第7、8、9组淋巴结穿刺。EUS还能穿刺活检左侧肾上腺、肝左叶以及腹腔淋巴结。因此,EUS-FNA 能够用于活检其他手段(如EBUS-TBNA、纵隔镜)所不能取到的淋巴结(如第8、9组淋巴结)。有些中心可使用EUS-FNA 穿刺活检第5、6组淋巴结,但是由于目前研究数据仍有限,我们不建议常规使用EUS-FNA 穿刺活检第5、6组淋巴结。对于为明确诊断的患者,穿刺的目标是获得尽量多的组织,提高诊断阳性率,而对于为明确纵隔淋巴结分期的患者,穿刺应至少探查第4R、4L及7组淋巴结,并且对于大于5mm 直径的淋巴结活检。为了避免穿刺针污染所致分期假阳性,淋巴结活检应当自N3淋巴结开始,随后按顺序活检N2、N1淋巴结。 诊断 胸部CT检查常可发现非钙化孤立性肺结节(SPNs),低剂量螺旋CT 筛查早期肺癌项目发现了许多孤立性肺结节。有研究提出,SPN 行PET 检查SUV 值大于25可作为恶性肿瘤的诊断标准,以此为标准,有综述发现SPN 大于10mm 的PET检查的敏感性、特异性、阳性预测值、阴性预测值和阴性似然比分别为0.95、0.81、0.90、0.90、0.06。而该综述同时提出,根据患者影像学分析评估结节的良恶性,敏感性和阴性似然比分别为0.98和0.02。SUV 值小于2.5就排除恶性肿瘤的结论目前广受争议,一项大型前瞻性研究指出,小于25mm 的SPN,24%仍为恶性肿瘤。另外,CT提示小于10mm 的或亚实型的磨玻璃结节,或者低代谢的结节(如类癌)也存在恶性的可能。因此,任何的PET 上FDG 高摄取的结节都应该进行临床上的综合评估,而不是基于SUV 最大值简单的界定划分。结节的综合评估包括临床特征(吸烟史、年龄),影像学特征以及结节的生长方式,综合评估可明显提高PET预测SPN的恶性可能性的准确性。 美国胸科医师学会(ACCP)研究指出,预计恶性程度小于10%的大于8mm 实性孤立肺结节,小于8mm 的实性孤立肺结节或者实性部分小于8mm 亚实性肺结节,均不建议行PET/CT检查。大于8mm 实性孤立肺结节或者实性部分大于8mm 亚实性结节预计恶性程度达到10%~60%时,行PET/CT 检查可以帮助确定患者是行进一步病理学检查明确还是保守观察治疗。实性或亚实性孤立肺结节预计恶性程度达到60%以上时,患者应行组织病理学诊断以及PET/CT检查明确TNM 分期。 由于细针穿刺活检有可能是唯一可获得肿块的组织学分型以及肺癌的基因分型的方式,近期专家共识建议细针穿刺活检应取尽可能多的组织。已证实可使用小组织样本通过现代病理学的取样切片测定及免疫组化的方式明确非小细胞肺癌分型,并且可使非小细胞肺癌不确定型(NOS)维持在20%以下。免疫组化提高了非小细胞肺癌分型的准确度,也提升了病理医生诊断的信心。细针穿刺标本行分子生物学分析是另一个需要关注的方面,有研究证实可使用细针穿刺的活检标本或涂片中提取DNA 样本,从而明确肿瘤存在的基因突变类型。 已有部分研究评估PET/CT作为肿瘤分期的标准检查的价值,共四项研究使用标准检查以及PET/CT进行肿瘤分期,其中三项研究以准确的TNM 分期为主要研究(表1),而另一项研究以“无益胸腔手术”率(良性疾病,开胸探查,病理学分期ⅢA-N2/ⅢB,或者在12月内复发、死亡)为终点,PET/CT 组“无益胸腔手术”率显著降低。PET/CT 的使用可指导患者治疗方案选择,如选择根治性治疗还是姑息性治疗,选择化疗还是其他治疗方法,PET/CT可增加4%~11%的Ⅳ期患者检出率。Maziak等研究发现PET/CT 可提高可切除的Ⅰ~Ⅲ期非小细胞肺癌分期的准确性。另一项加拿大的研究,纳入不可切除Ⅲ期非小细胞肺癌患者,140例患者行PET/CT检查,发现21例(15%)患者分期上调,而149例行CT 检查的患者仅4例(2.7%)分期上调,两组患者差异具有显著性(P=0.0002)。目前所有的证据都认为,PET/CT 相比于传统检查分期可明显提高准确率,从而使患者治疗方案选择优化,以及可能的生存获益。有随机对照研究评估全身1.5T MRI/PET与PET/CT联合头颅MRI对于Ⅰ~Ⅲ期肺癌分期的准确性,结果显示相对于单独使用肺部CT 扫描,两种方法可上调20%患者分期,相比于PET/CT,1.5T MRI/PET检查可导致更多的不必要的创伤性检查,且在评估胸腔外远处转移没有优势。 表1PET/CT评估TNM分期的随机对照研究列表 增强CT可以明确肿瘤与纵隔、胸膜或者胸壁组织的界限,确定肿瘤临床T分期,指导手术切除范围。PET/CT 可准确区分肿瘤与肿瘤周围的炎症和肺不张。对于N分期,Meta分析指出,PET/CT相对于单独的CT 对于淋巴结分期准确性更高,敏感度为76%,特异度为88%,阴性似然比为0.28,阳性似然比为6.4,提示PET/CT纵隔淋巴结阴性不能完全排除纵隔淋巴结转移,而PET/CT纵隔淋巴结阳性同样不能确定存在淋巴结转移。由于PET/CT 诊断纵隔淋巴结转移的阴性预测值(NPV)较高,因此对于PET/CT 提示纵隔淋巴结阴性,原发肿瘤小于3cm 的患者可不行有创性的淋巴结分期检查,PET/CT还可以帮主确定可疑淋巴结的位置,为EBUS-TBNA,EUS-FNA 或纵隔镜定位。对于M分期,PET/CT明显优于单独使用CT,但是由于脑部正常组织的糖摄取量较高,因此PET/CT评估颅内转移灶敏感性较低。PET 评估骨转移较99mTcMDP骨扫描准确性更高。对于肾上腺转移,PET 诊断肾上腺转移敏感性高,因此CT 提示肾上腺占位,而PET提示代谢低则转移可能性低。PET也能帮助确定常规检查中诊断不明的肝脏占位。PET还能显示常见转移部位以外的占位,如软组织占位、腹膜后淋巴结、锁骨上淋巴结、无痛骨占位等。PET/CT 诊断多发转移灶的价值无可替代,但由于存在假阳性或第二原发肿瘤可能,PET检查发现的孤立性转移灶仍需其他进一步的检查或病理学活检已明确,是当PET/CT 检出可疑的孤立占位时,需要其他的检查或者组织学活检经行确定,因为存在假阳性或者第二原发肿瘤的可能性。 超声内镜纵隔淋巴结分期(N分期) 纵隔镜检查曾被作为纵隔淋巴结分期检查的金标准,但目前正在受到EBUS和EUS的挑战。多篇Meta分析研究显示,EUS-FNA、EBUS-FNA 及EUS-FNA+EBUS-TBNA 的诊断敏感度为83%~94%。目前已有3项对照研究结果发表,其中两项在2007年ESTS指南中提及,比较了EUS-FNA、EBUS-FNA、EUS-FNA+EBUS-TBNA、纵隔镜、超声内镜+纵隔镜检查诊断纵隔淋巴结分期的准确性,结果见图2,EUS-FNA+EBUS-TBNA 检查敏感度为0.94(95% CI 0.85~0.98),明显高于单纯经颈部纵隔镜检查(0.79,95% CI 0.66~0.88,P=0.02)。最近有Meta分析结果显示超声内镜阴性似然比为0.15,提示超声内镜检查淋巴结阴性的患者中,有15%的患者可能有纵隔淋巴结转移,这个比例依然偏高,导致很多患者不能行解剖性根治性切除,因此对于超声内镜检查提示淋巴结阴性的患者仍需行外科手术已明确淋巴结分期。另有一项随机对照研究纳入153例Ⅰ~Ⅲ期肺癌患者,比较超声内镜和纵隔镜评估淋巴结分期的价值,结果显示两者敏感度及阴性似然比均无显著性差异,需要指出的是,该研究中患者纵隔淋巴结转移率低于其他研究,EBUS-TBNA 对29%的纵隔淋巴结取样不够充分,纵隔镜及EBUS-TBNA 的敏感度分别为0.79(95% CI 0.62~0.87),0.81(95% CI 0.68~0.90),阴性预测值分别为,0.90(95% CI 0.83~0.95),0.91(95% CI 0.84~0.95),EBUS-TBNA 及纵隔镜联合检查的敏感度为0.92(95% CI 0.81~0.98),阴性预测值为0.96(95% CI 0.90~0.99)。最近的一项研究比较了2种超声内镜方式(EBUS、EUS)的区别,发现两者没有显著差异,但EUS联合EBUS可以明显提高诊断分期的准确性和敏感性,该研究建议可将EBUS作为初始诊断方法,而后可使用EUS进一步诊断。 图2多项临床试验比较纵隔镜、EBUS-TBNA、EBUS+EUS、ES+ 纵隔镜应用于可切除Ⅰ~Ⅲ 期肺癌纵隔淋巴结分期的敏感性结果。ES:EBUS+EUS。Yasufuku等,Annema等,Kang等 超声内镜下穿刺活检对于诊断评估Ⅰ~Ⅲ期肺癌纵隔淋巴结分期有效可减少50%以上的外科有创性淋巴结分期检查的使用,EBUS-TBNA 联合EUS-FNA检查安全,并发症发生率小于1%。 《肺癌诊治新进展》 原著者:Solange PetersBenjamin Besse 主译:胡坚 副主译:汪路明包飞潮 北京:科学出版社,2017.4 ISBN:978-7-03-052499-7 可购买本书 肺癌是目前全球死亡率最高的恶性肿瘤,其诊治涉及胸外科、肿瘤科、放疗科、放射科等多个学科,原先的单一学科治疗肺癌的模式已经难以适应新时代肺癌的诊治要求,目前必须通过多学科诊治方能提高治疗效果。《肺癌诊治新进展》主要内容共分为五个部分,即诊断新进展、早期非小细胞肺癌治疗新进展、局部晚期非小细胞肺癌治疗新进展、分子治疗进展、特定类型转移性非小细胞肺癌诊治进展,参考了最新发表的关于肺癌外科微创治疗、放射治疗、化学治疗、靶向治疗、免疫治疗等领域相关文献及有突破意义的临床研究,观点新颖,内容科学,力求全面展现肺癌诊治的最新面貌,符合肺癌专科医生的实际需求,是一本不可多得的专著。


曾任美国临床肿瘤学会(ASCO)临床实践指南委员会主席
约翰霍普金斯医学院,医学博士
Lifespan癌症研究所胸部肿瘤科主任
曾在纽约纪念斯隆凯特琳癌症中心任职10年
曾在波士顿的麻省总医院癌症中心任职6年

 400-107-6696
400-107-6696



 海堰
海堰
 12529
12529
 0
0

 19758
19758






 京公网安备 11010502037180号
京公网安备 11010502037180号
 400-107-6696
400-107-6696


